政策法規 || 《藥品審評中心藥物臨床試驗期間安全信息評估與風險管理工作程序(試行)修訂稿(征求意見稿)》(附近期法規概覽)
01
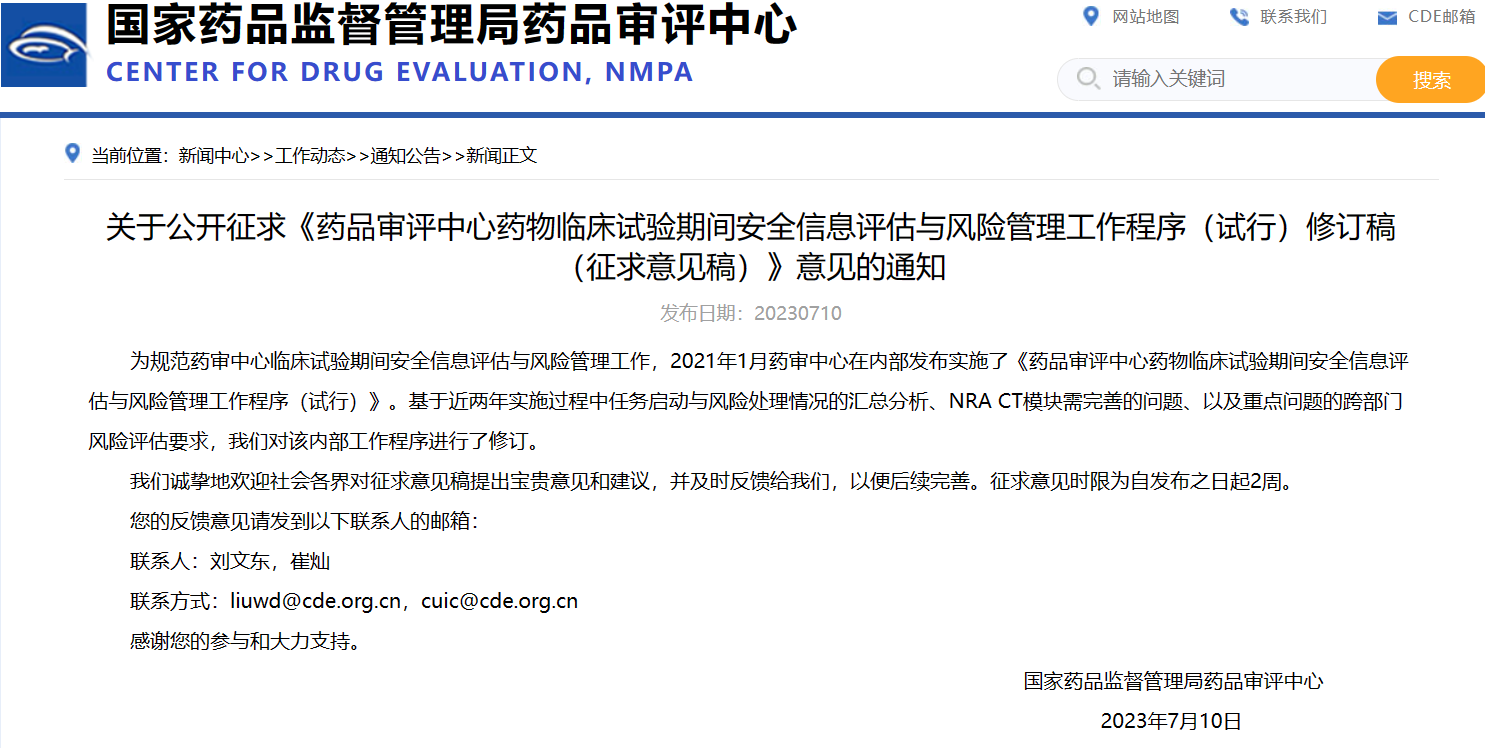
關于公開征求《藥品審評中心藥物臨床試驗期間安全信息評估與風險管理工作程序(試行)修訂稿(征求意見稿)》意見的通知
掃描識別圖中二維碼
查看詳細信息

02
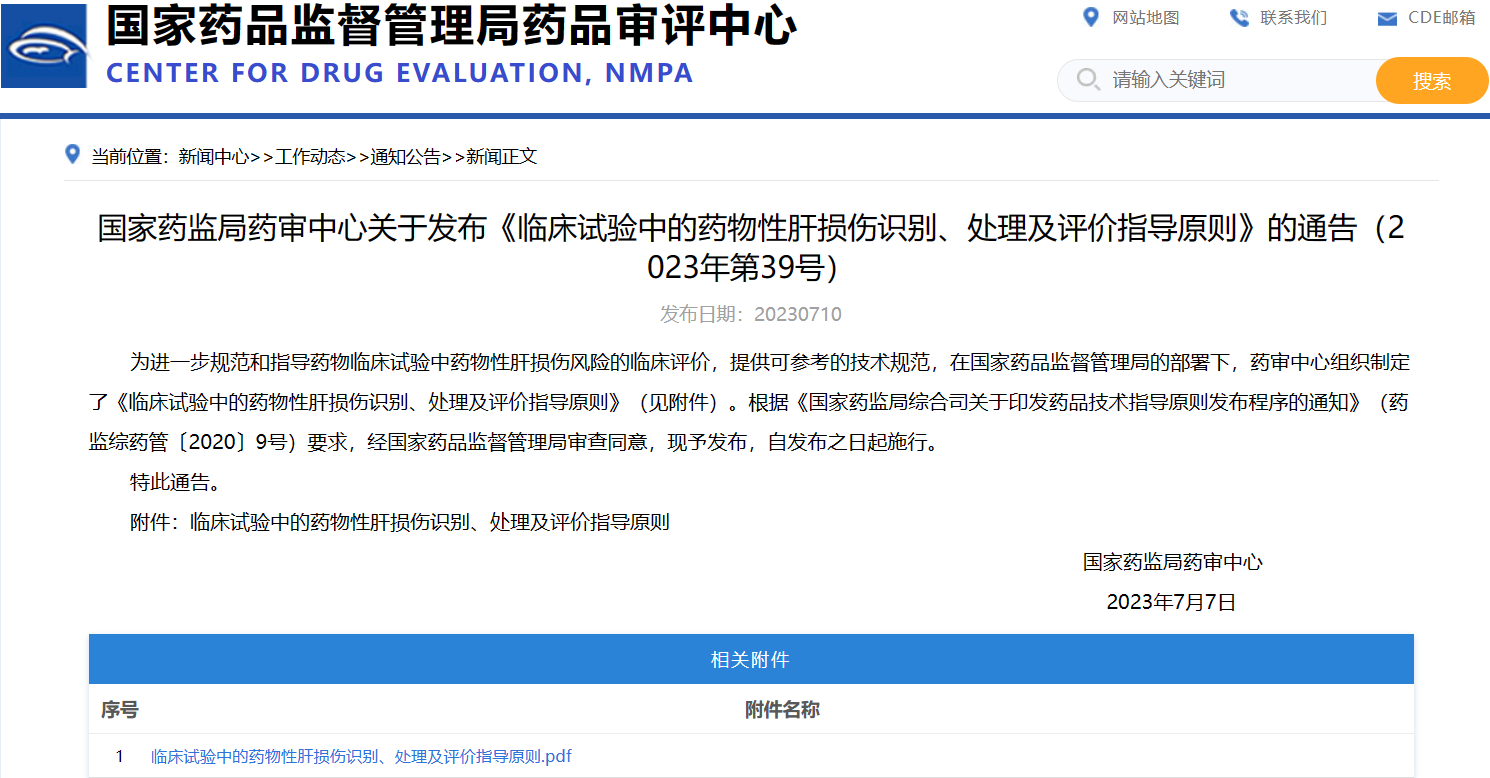
國家藥監局藥審中心關于發布《臨床試驗中的藥物性肝損傷識別、處理及評價指導原則》的通告(2023年第39號)
掃描識別圖中二維碼
查看詳細信息

03
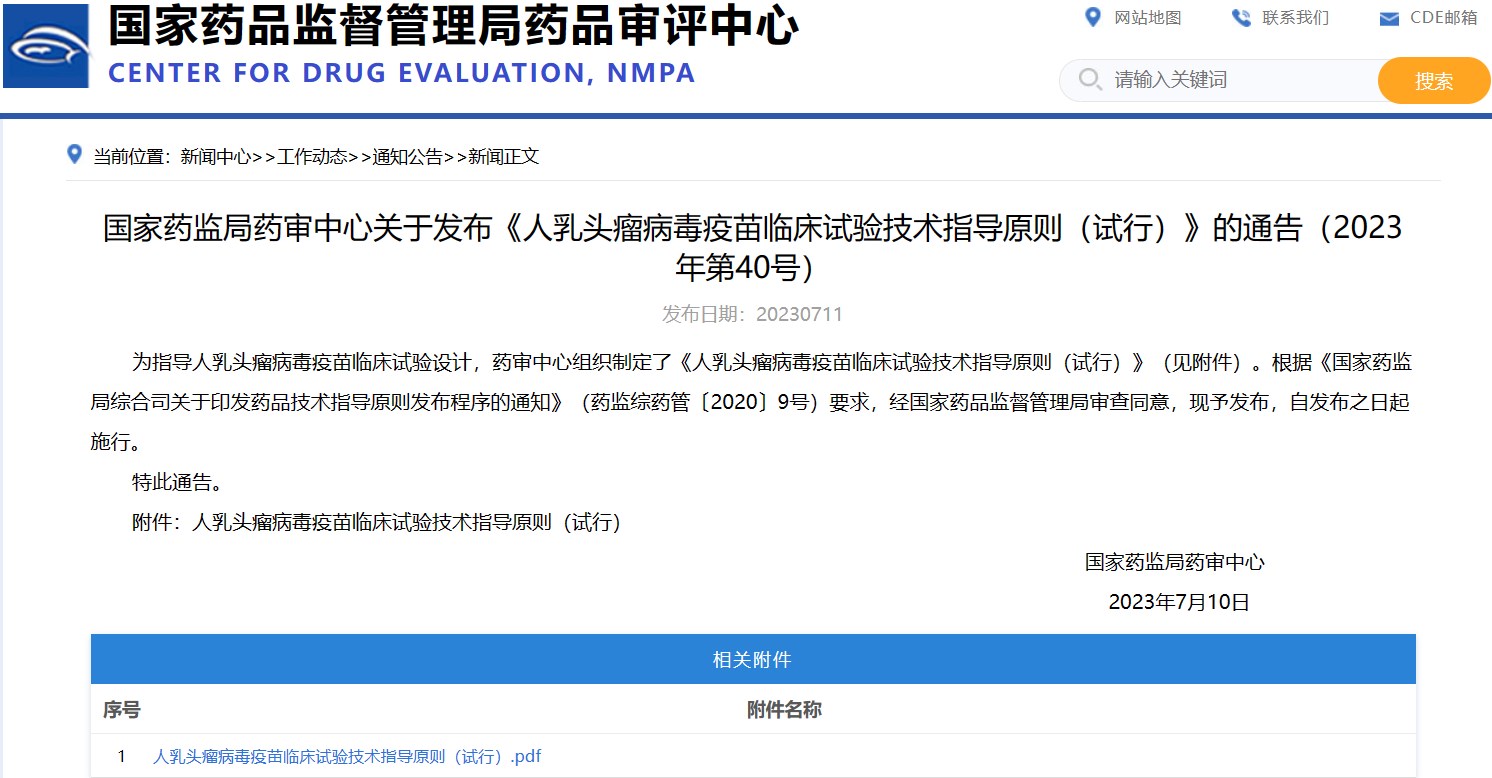
國家藥監局藥審中心關于發布《人乳頭瘤病毒疫苗臨床試驗技術指導原則(試行)》的通告(2023年第40號)
掃描識別圖中二維碼
查看詳細信息

NMPA
01
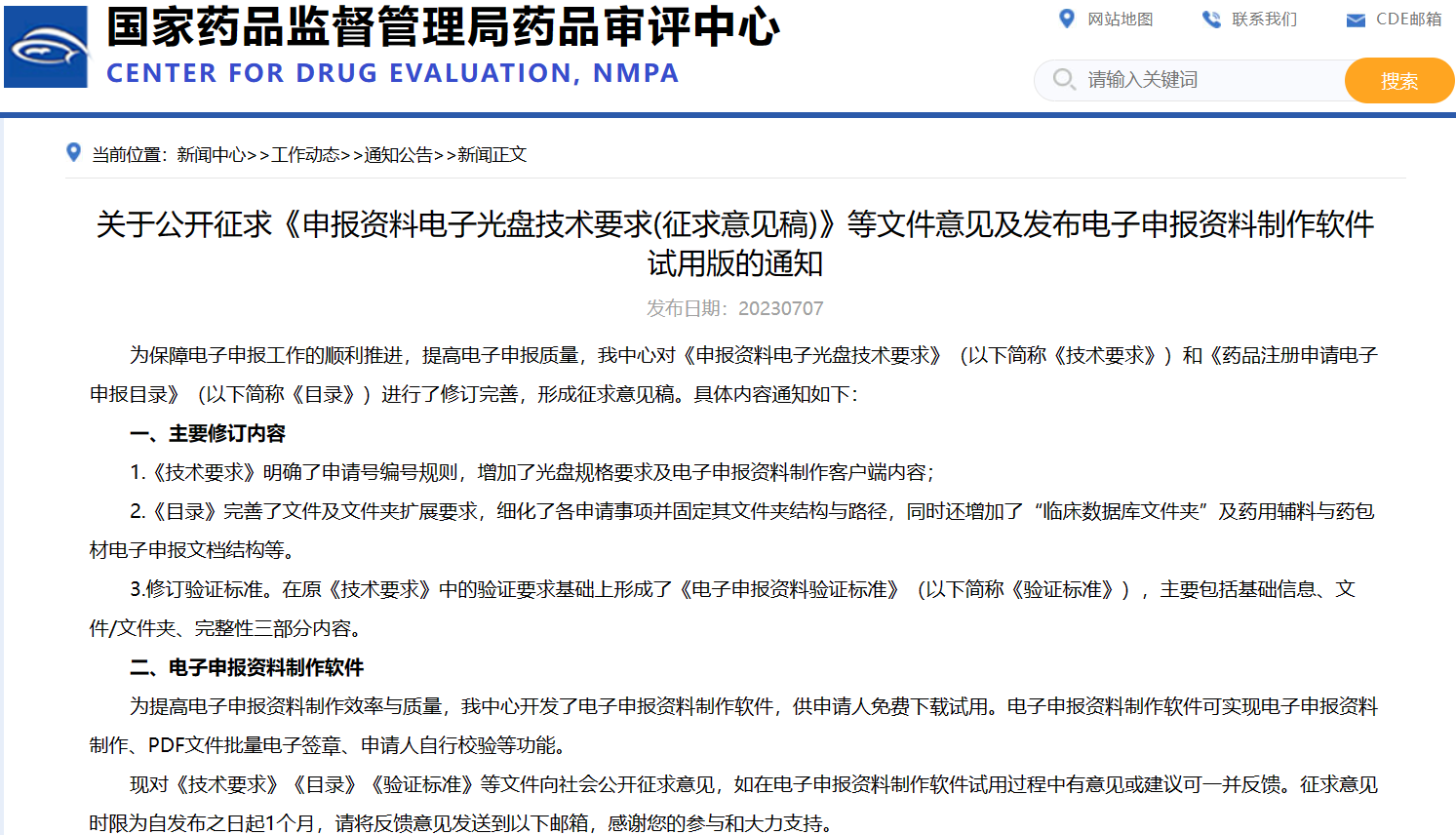
關于公開征求《申報資料電子光盤技術要求(征求意見稿)》等文件意見及發布電子申報資料制作軟件試用版的通知
掃描識別圖中二維碼
查看詳細信息

02
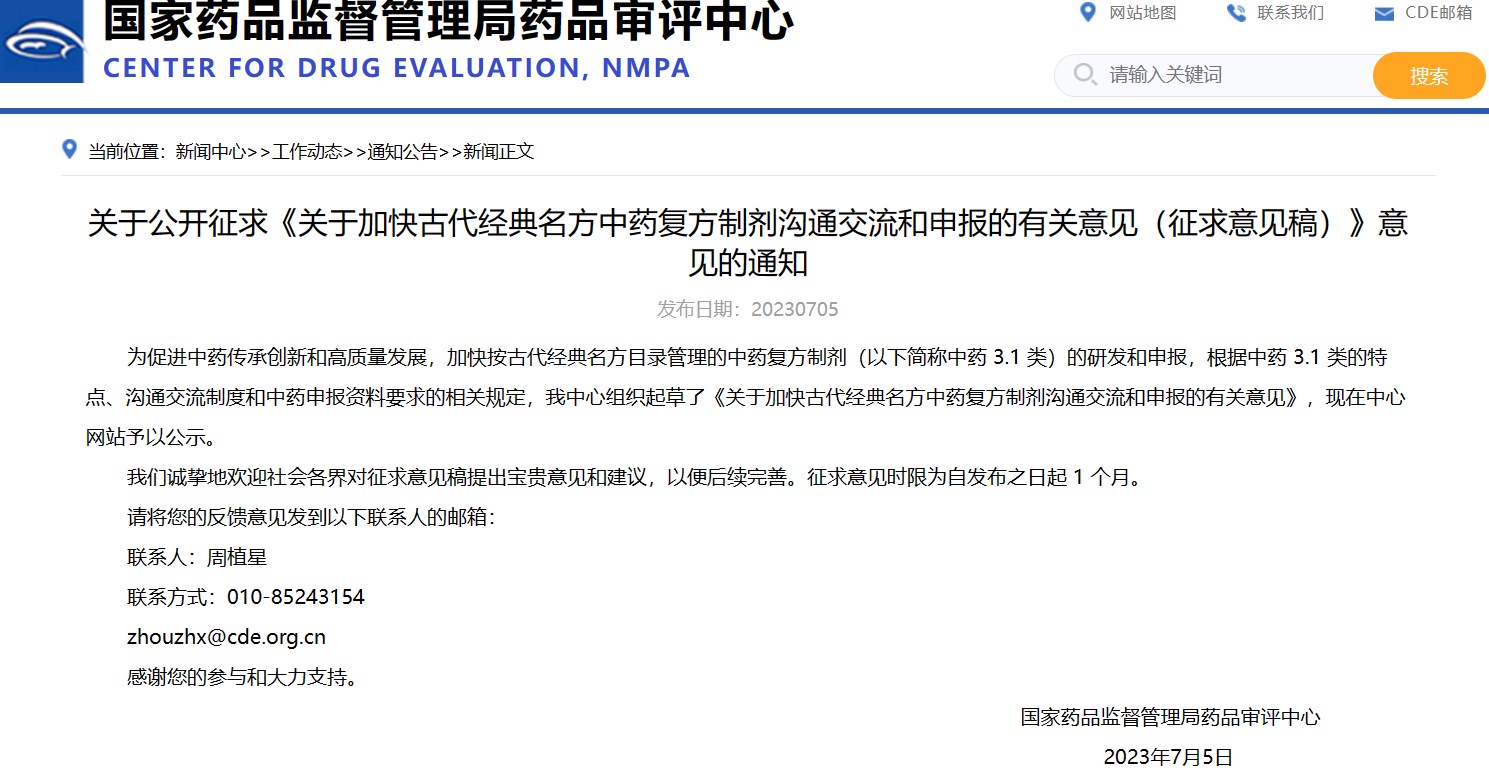
關于公開征求《關于加快古代經典名方中藥復方制劑溝通交流和申報的有關意見(征求意見稿)》意見的通知
掃描識別圖中二維碼
查看詳細信息

03
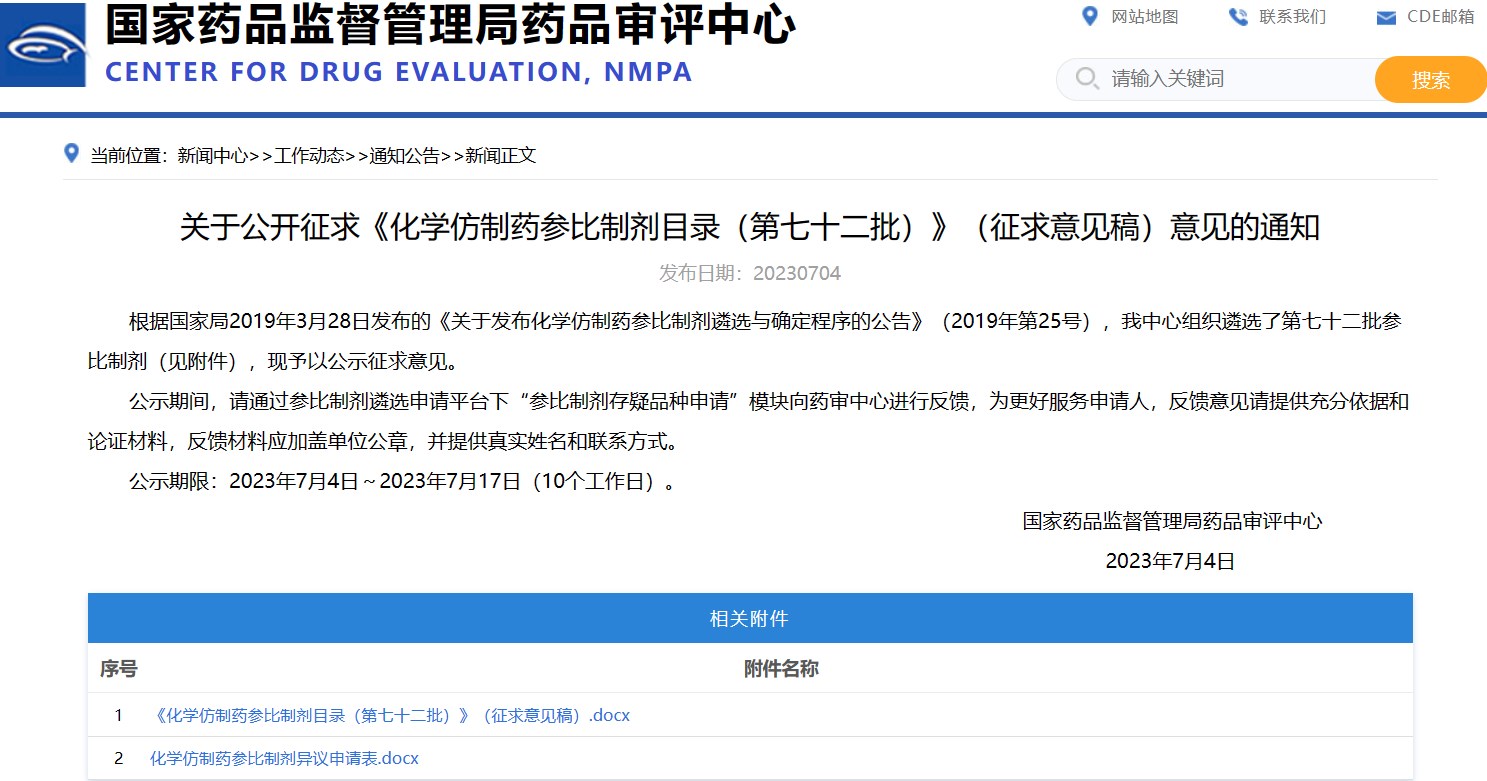
關于公開征求《化學仿制藥參比制劑目錄(第七十二批)》(征求意見稿)意見的通知
掃描識別圖中二維碼
查看詳細信息

04
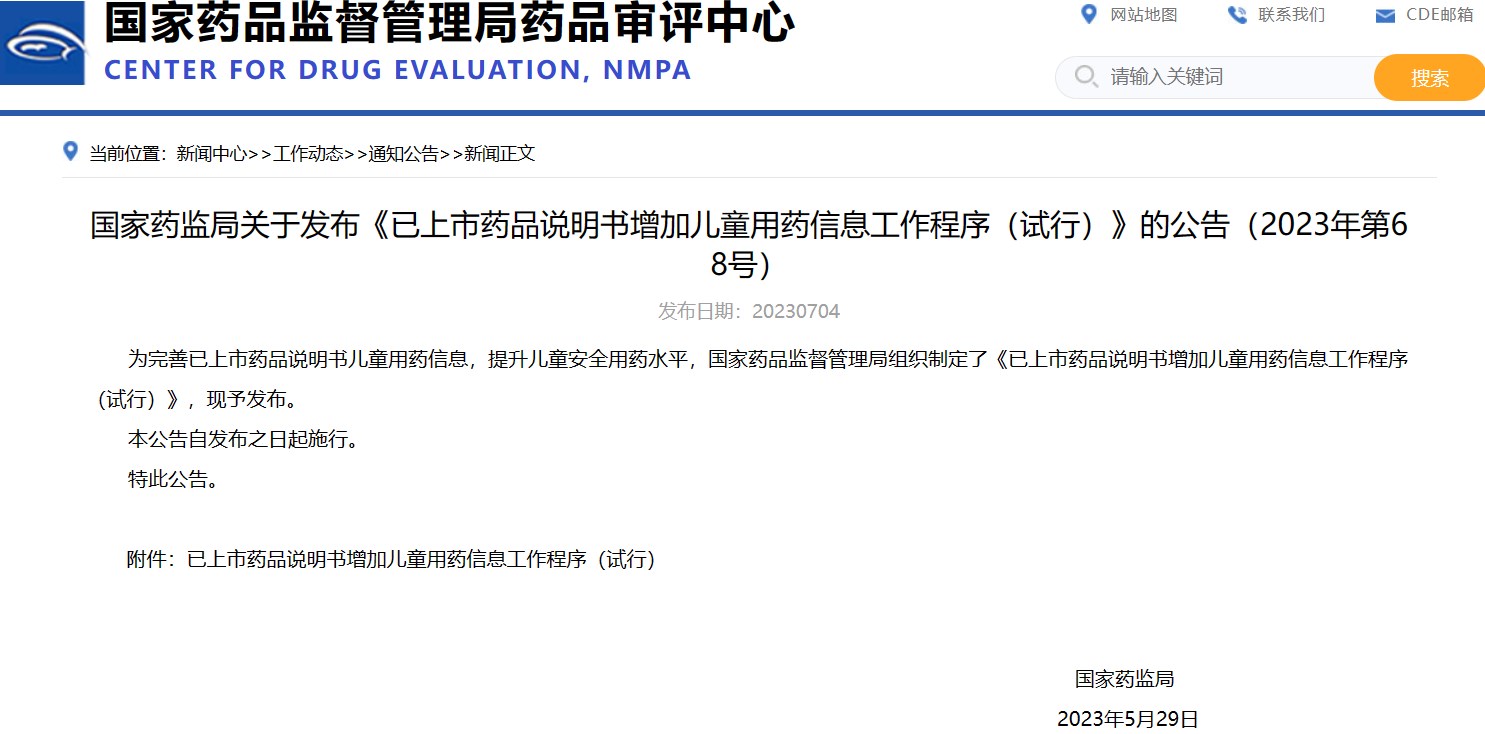
國家藥監局關于發布《已上市藥品說明書增加兒童用藥信息工作程序(試行)》的公告(2023年第68號)
掃描識別圖中二維碼
查看詳細信息

05
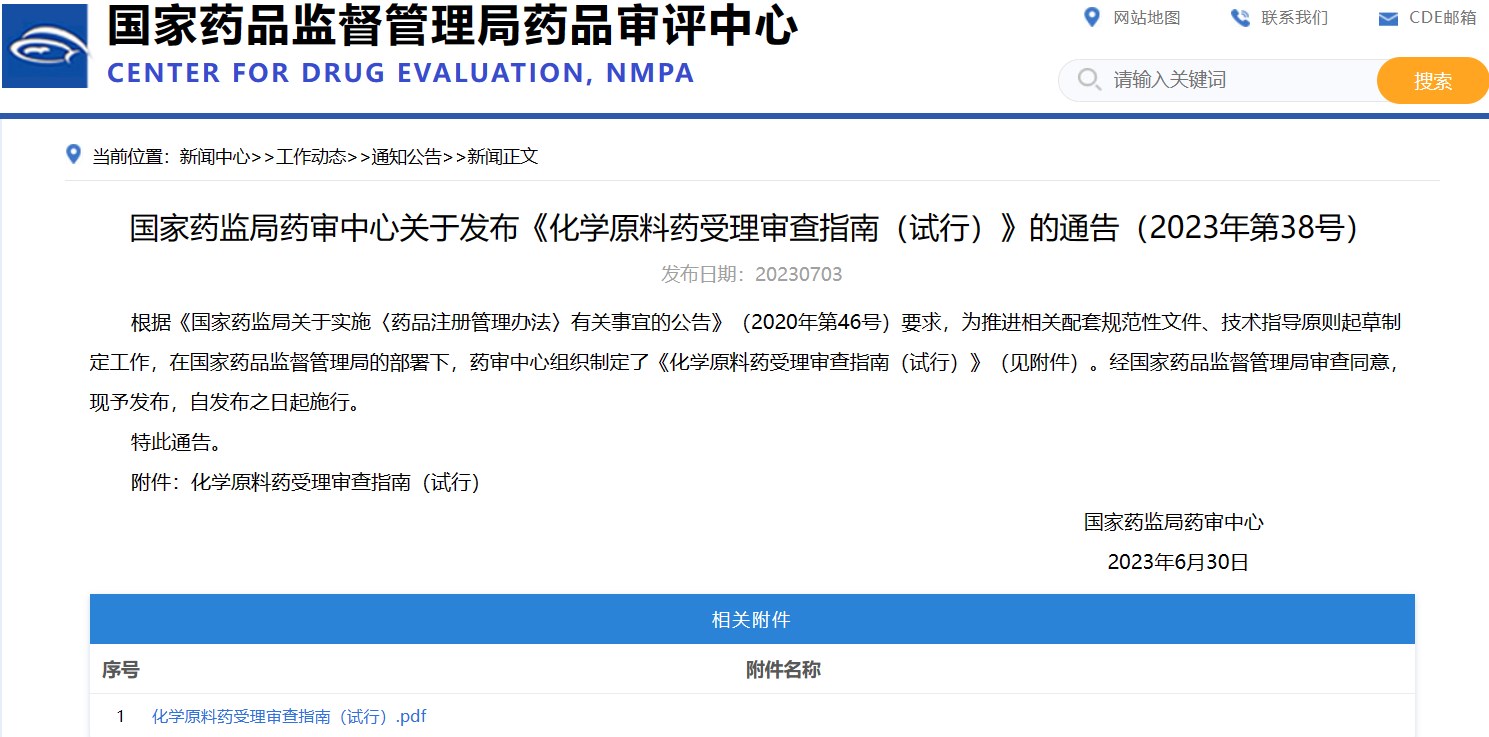
國家藥監局藥審中心關于發布《化學原料藥受理審查指南(試行)》的通告(2023年第38號)
掃描識別圖中二維碼
查看詳細信息

06
2023年07月11日中藥品種保護受理公示

掃描識別圖中二維碼
查看詳細信息

07
國家藥監局關于發布《藥品標準管理辦法》的公告(2023年第86號)
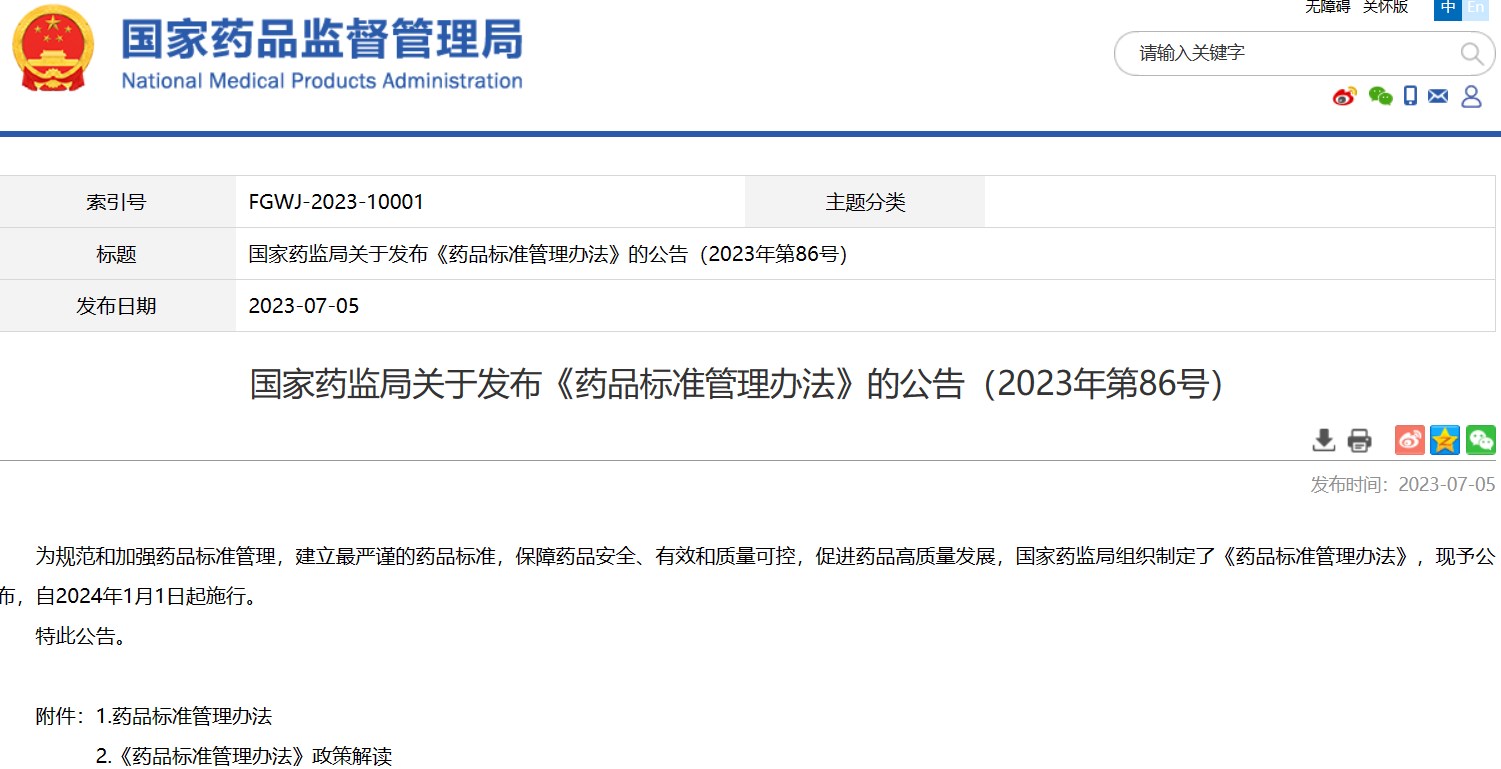
掃描識別圖中二維碼
查看詳細信息

08
國家藥監局關于適用《M10:生物分析方法驗證及樣品分析》國際人用藥品注冊技術協調會指導原則問答文件和常見問題解答文件的公告(2023年第84號)

掃描識別圖中二維碼
查看詳細信息

非處方藥轉換眾生片的公示
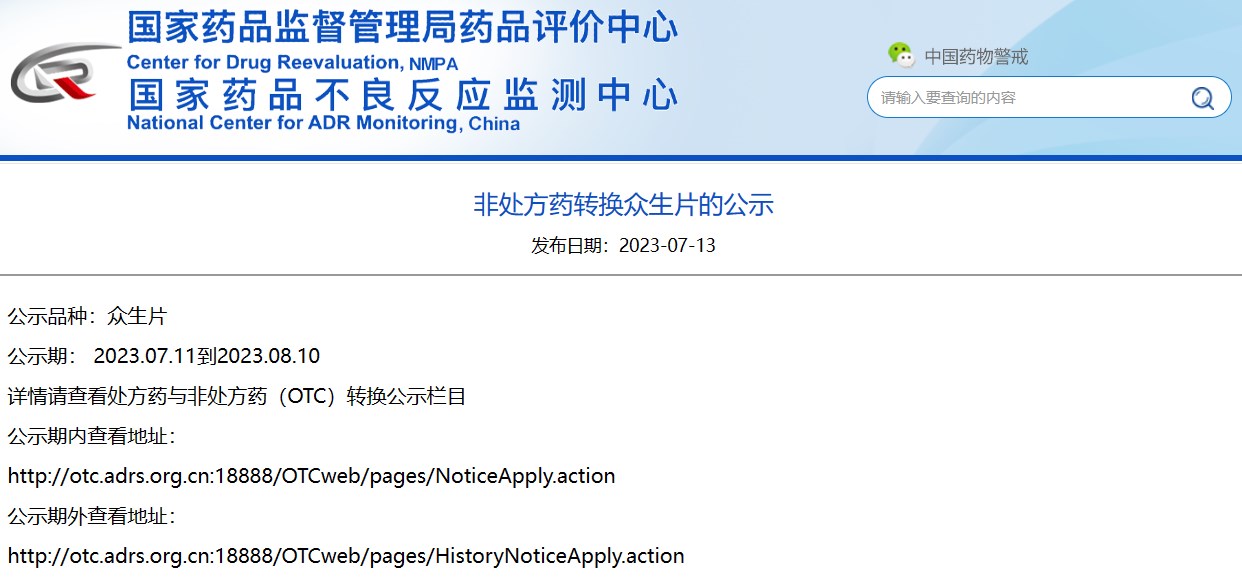
掃描識別圖中二維碼
查看詳細信息

-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
